תוכן
טיפול גנטי
שימוש בגנים כתרופה: זה הרעיון מאחורי הטיפול הגנטי. אסטרטגיה טיפולית המורכבת משינוי גנים לריפוי מחלה, הריפוי הגנטי נמצא עדיין בחיתוליו אך התוצאות הראשונות שלו מבטיחות.
מהו טיפול גנטי?
הגדרה של ריפוי גנטי
טיפול גנטי כרוך בשינוי גנטי של תאים כדי למנוע או לרפא מחלות. היא מבוססת על העברה של גן טיפולי או העתק של גן פונקציונלי לתאים ספציפיים, במטרה לתקן פגם גנטי.
העקרונות העיקריים של ריפוי גנטי
כל אדם מורכב מכ-70 מיליארד תאים. כל תא מכיל 000 זוגות של כרומוזומים, המורכבים מחוט בצורת סליל כפול, DNA (חומצה דאוקסיריבונוקלאית). ה-DNA מחולק לכמה אלפי חלקים, גנים, מהם אנו נושאים כ-23 עותקים. גנים אלו מרכיבים את הגנום, מורשת גנטית ייחודית המועברת על ידי שני ההורים, המכילה את כל המידע הדרוש להתפתחות הגוף ותפקודו. הגנים אכן מציינים לכל תא את תפקידו באורגניזם.
מידע זה מועבר הודות לקוד, שילוב ייחודי של 4 הבסיסים החנקניים (אדנין, תימין, ציטוזין וגואנין) המרכיבים את ה-DNA. בעזרת קוד, ה-DNA מייצר RNA, השליח המכיל את כל המידע הדרוש (הנקרא אקסונים) לייצור חלבונים, שכל אחד מהם ישחק תפקיד מסוים בגוף. כך אנו מייצרים עשרות אלפי חלבונים החיוניים לתפקוד הגוף שלנו.
שינוי ברצף של גן משנה אפוא את ייצור החלבון, שאינו יכול עוד למלא את תפקידו בצורה נכונה. בהתאם לגן המעורב, זה עלול להוביל למגוון רחב של מחלות: סרטן, מיופתיה, סיסטיק פיברוזיס וכו'.
עקרון הטיפול הוא אפוא לספק, הודות לגן טיפולי, קוד נכון כך שהתאים יוכלו לייצר את החלבון החסר. גישת גנים זו כרוכה תחילה בהכרה מדויקת של מנגנוני המחלה, הגן המעורב ותפקיד החלבון עבורו היא מקודדת.
היישומים של ריפוי גנטי
מחקר ריפוי גנטי מתמקד במחלות רבות:
- סרטן (65% מהמחקר הנוכחי)
- מחלות מונוגניות, כלומר מחלות המשפיעות על גן אחד בלבד (המופיליה B, תלסמיה)
- מחלות זיהומיות (HIV)
- מחלות לב וכלי דם
- מחלות נוירודגנרטיביות (מחלת פרקינסון, מחלת אלצהיימר, אדרנוקודיסטרופיה, מחלת סנפיליפו)
- מחלות דרמטולוגיות (צומת אפידרמוליזיס בולוזה, אפידרמוליזיס דיסטרופית)
- מחלות עיניים (גלאוקומה)
- וכו '
רוב הניסויים עדיין במחקר שלב I או II, אך חלקם כבר הביאו לשיווק תרופות. אלו כוללים:
- Imlygic, האימונותרפיה האונקוליטית הראשונה נגד מלנומה, שקיבלה את אישור השיווק שלה (אישור שיווק) בשנת 2015. היא משתמשת בנגיף הרפס סימפלקס-1 מהונדס גנטית כדי להדביק תאים סרטניים.
- Strimvelis, הטיפול הראשון המבוסס על תאי גזע, קיבל את אישור השיווק שלו בשנת 2016. הוא מיועד לילדים הסובלים מאלימפוציטוזיס, מחלה חיסונית גנטית נדירה ("תסמונת "תינוק בועה").
- התרופה Yescarta מיועדת לטיפול בשני סוגים של לימפומה אגרסיבית שאינה הודג'קין: לימפומה מפוזרת של תאי B גדולים (LDGCB) ולימפומה ראשונית של תאי B מסוג B עמידים או חוזרים (LMPGCB). היא קיבלה את אישור השיווק שלה ב-2018.
ריפוי גנטי בפועל
קיימות גישות שונות בריפוי גנטי:
- החלפת גן חולה, על ידי ייבוא עותק של גן פונקציונלי או "גן טיפולי" לתא מטרה. זה יכול להיעשות גם in vivo: הגן הטיפולי מוזרק ישירות לגוף המטופל. או במבחנה: תאי גזע נלקחים מחוט השדרה, משתנים במעבדה ואז מוזרקים מחדש לחולה.
- עריכה גנומית מורכבת מתיקון ישיר של מוטציה גנטית בתא. אנזימים, הנקראים נוקלאזות, יחתכו את הגן במקום המוטציה שלו, ואז קטע של DNA מאפשר לתקן את הגן שהשתנה. עם זאת, גישה זו עדיין ניסיונית בלבד.
- שינוי RNA, כך שהתא מייצר חלבון פונקציונלי.
- השימוש בווירוסים מותאמים, הנקראים אונקוליטים, כדי להרוג תאים סרטניים.
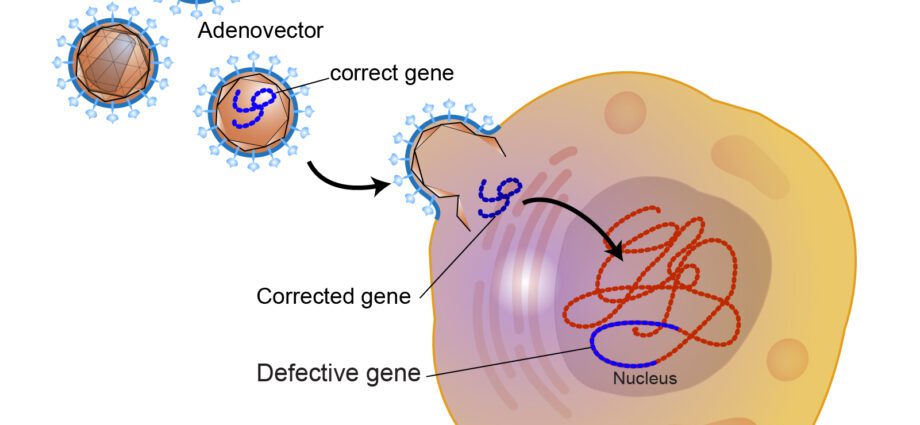
כדי להכניס את הגן הטיפולי לתאי המטופל, טיפול גנטי משתמש במה שנקרא וקטורים. הם לרוב וקטורים ויראליים, שהפוטנציאל הרעיל שבהם בוטל. חוקרים עובדים כעת על פיתוח וקטורים לא ויראליים.
היסטוריה של ריפוי גנטי
זה היה בשנות ה-1950, הודות לידע טוב יותר של הגנום האנושי, שהמושג של ריפוי גנטי נולד. עם זאת, נדרשו כמה עשורים כדי להשיג את התוצאות הראשונות, שאנו חייבים לחוקרים צרפתים. בשנת 1999, אלן פישר וצוותו ב-Inserm הצליחו לטפל ב"בועות תינוקות" הסובלות ממחסור חיסוני משולב חמור הקשור לכרומוזום X (DICS-X). הצוות אכן הצליח להחדיר עותק תקין של הגן שהשתנה לגופם של ילדים חולים, באמצעות וקטור ויראלי מסוג רטרו-וירוס.